Конспект урока химии, 11 класс. Водородный показатель
Конспект урока химии по теме: «Водородный показатель», 11 класс
Автор: Таирова Елена Александровна, учитель химии МБОУ гимназия 44 г. ПензыДанная разработка конспекта урока предназначена для учителей химии. Материал позволяет провести интересный урок изучения нового материала в 11 классе с использованием технологии развития критического мышления через чтение и письмо, технологии проблемного урока.
Цель: создание условий для формирования понятия водородный показатель.
Задачи:
Образовательные.
1. Познакомить учащихся с понятием ионного произведения воды; концентрациями ионов Н+ и в кислых, нейтральных и щелочных растворах; с водородным показателем - отрицательным логарифмом концентрации; с методами определения рН.
2. Актуализировать знаний учащихся о реакции среды растворов кислот, щелочей, солей; изменении цвета индикаторов (лакмуса, метилового оранжевого, фенолфталеина) в различных средах.
3. Измерить с учащимися рН некоторых растворов с помощью универсального индикатора: дистиллированной, газированной воды, раствора уксуса, сока лимона, раствора аммиака, раствора мыла, средства для прочистки труб, раствора питьевой соды; подвести учащихся к объяснению причин значений рН данных растворов.
4. Опытным путем (в ходе домашнего эксперимента) доказать, что соки некоторых растений так же могут служить кислотно - основными индикаторами (на примере сока краснокочанной капусты).
Воспитательные.
Способствовать развитию творческого отношения к учебной деятельности; воспитание аккуратности и внимательности при выполнении работ с кислыми и щелочными растворами.
Развивающие.
Развивать навыки самостоятельного умственного труда: совершенствовать умения самостоятельно получать информацию из учебного текста, анализировать текст, формировать критический стиль мышления; развивать практические умения проводить эксперимент.
Оборудование: датчик рН, подключенный к компьютеру, проектор, учебные тексты (по одному на парту), лотки со штативами для пробирок и нумерованными пробирками с бытовыми растворами (по одному на парту).
Реактивы: растворы индикаторов – лакмуса, метилоранжа, фенолфталеина, универсальная индикаторная бумага, бытовые растворы - газированная вода, растворы уксуса, сока лимона, аммиака, мыла, средства для прочистки труб, питьевой соды, дистиллированная вода.
Ход урока:
Организационный момент- Здравствуйте, ребята! Я рада встрече с вами, желаю вам хорошего настроения и плодотворной работы.
Фаза вызов
-Ребята, давайте составим кластер «Реакция среды растворов».
Ученик на доске составляет кластер
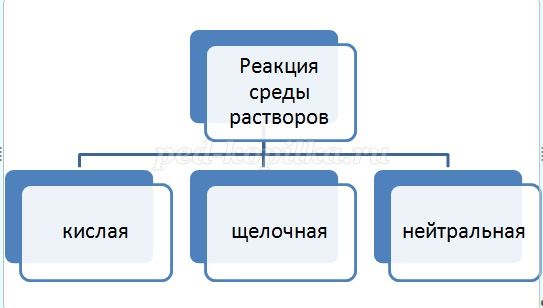
Индикаторами.
Какие индикаторы вы знаете?
- Лакмус, метилоранж, фенолфталеин.
-Как изменяются их цвета в зависимости от реакции среды? Составьте кластеры.
Ученики у доски составляют кластеры.
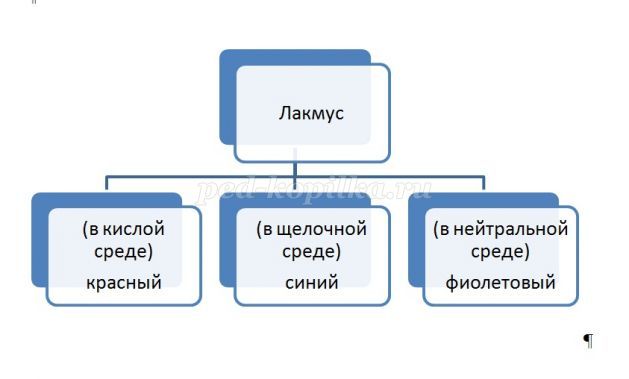
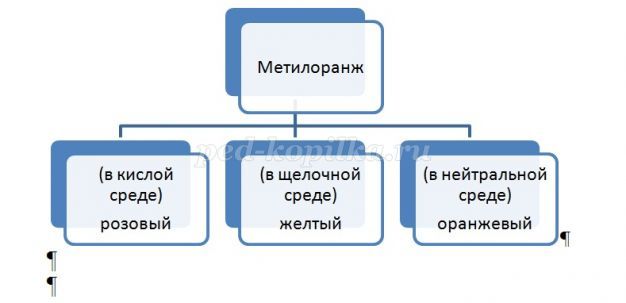
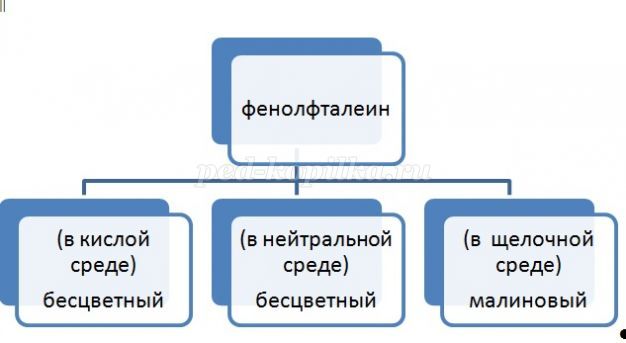
• Раствор уксуса менее кислый, чем сок лимона.
• Раствор мыла более щелочной, чем раствор питьевой соды.
Одни ребята говорят, что верят, а другие, что нет.
- Сколько же в нашем классе мнений? (побуждение к осознанию противоречия)
- Два разных мнения (осознание противоречия)
- Какой возникает вопрос? (побуждение к формулированию учебной проблемы)
-Как доказать точно, какой раствор более кислый, а какой более щелочной? (учебная проблема как вопрос)
- Так, как вы думаете, как же это можно сделать? Давайте проведем мозговой штурм.
- На вкус.
- Так, все согласны?
- Нельзя пробовать вещества в химической лаборатории.
- При помощи индикаторов, по интенсивности их окраски.
- Так, все согласны?
- Да.
- Тогда давайте попробуем. Поработайте в парах, определите реакцию среды при помощи индикаторов некоторых бытовых растворов, налитых в нумерованные пробирки, расположенные у вас на столах: уксуса, раствора аммиака, лимонного сока, газированной воды, средства для прочистки водосточных труб, раствора мыла, раствора питьевой соды, дистиллированной воды. Первый ряд исследует растворы лакмусом, второй – метилоранжем, третий – фенолфталеином. Затем все вместе заполняем таблицу:
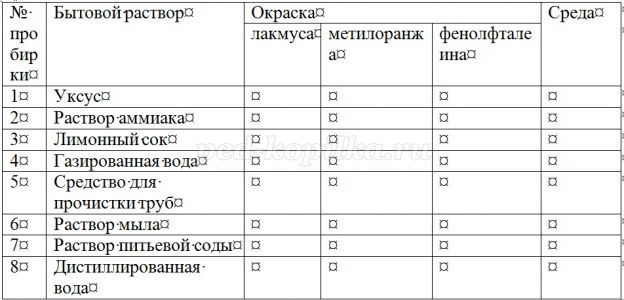
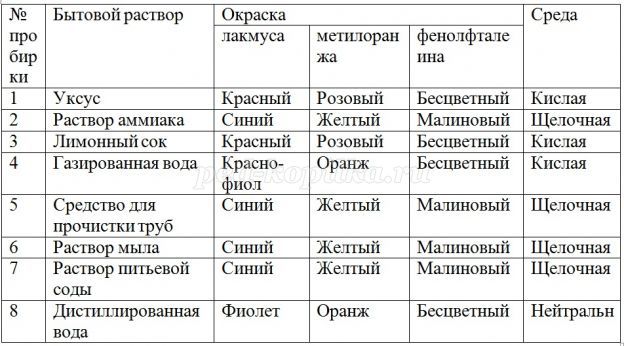
- Нет, интенсивность окраски индикатора была одинаковая.
- Так, давайте ещё подумаем, когда удается сравнить величины?
- Когда есть количественное значение.
- Давайте подумаем, что же можно измерить? Какие частицы определяют кислую реакцию среды?
- Катионы водорода - H+
-Хорошо, как они образовались в исследуемых нами кислых бытовых растворах?
Ученики на доске записывают уравнения реакций диссоциации уксусной и лимонной кислот, угольной кислоты, образовавшейся при взаимодействии углекислого газа с водой.
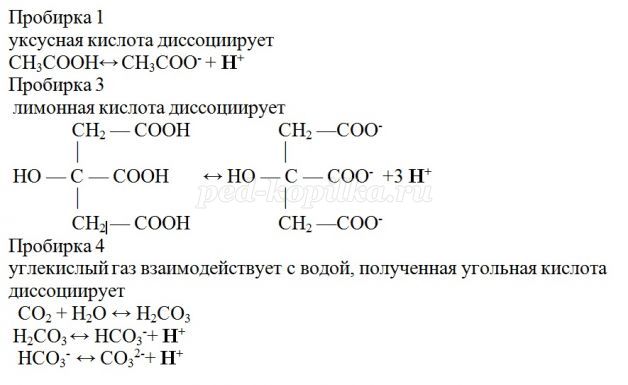
- Наличие гидроксид-ионов - OH-
-Хорошо, как они образовались в исследуемых нами щелочных бытовых растворах?
Ученики у доски объясняют наличие гидроксид-ионов в щелочных растворах.

- Молекулы воды.
- Нет, не только вода нейтральна, наверное отсутствие катионов водорода или гидроксид – ионов.
Ученики высказывают разные мнения, затрудняются с определением правильной версии.
- Ответить на этот и другие поставленные в ходе урока вопросы мы сможем, изучив учебный текст.
Фаза осмысление
Учитель предлагает ученикам учебный текст:



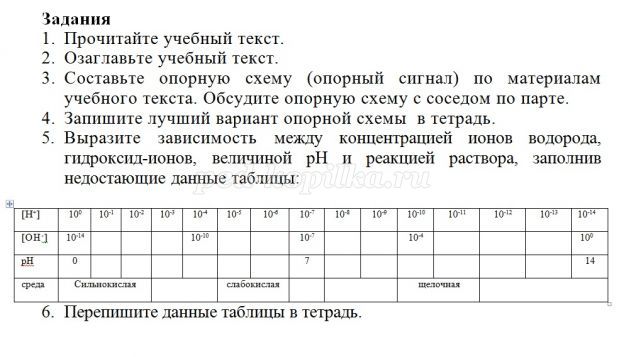
Рефлексия.
-Ребята, давайте сформулируем тему сегодняшнего урока. Какие варианты заголовка текста вы предложите?
- Количественная характеристика кислотности или основности.
- Диссоциация воды. рН
- Водородный показатель.
- Хорошо, тема нашего урока – «Водородный показатель».
- Какие варианты опорных схем вы можете предложить?
После обсуждения вариантов опорных сигналов останавливаемся на опоре такого вида, записываем её на доске:

Четыре ученика у доски демонстрационно измеряют рН бытовых растворов уксуса, сока лимона, раствора мыла, раствора питьевой соды.
- Получилось узнать, что кислее, уксус или лимон?
- Нет, окраска индикаторной бумаги одинаковая, рН в районе 2-3, точнее определить не удается.
- Получается определить, какой раствор более щелочной – мыла или питьевой соды?
-Да, раствор мыла более щелочной, рН 10, а раствор питьевой соды менее щелочной, рН 9.
- Почему не получилось выяснить, какой раствор кислее?
- Точность определения значения рН при помощи универсального индикатора равна единице, т.е. мы находим довольно неточное значение рН раствора.
- Действительно, более точное значение рН можно измерить цифровым датчиком рН, подключенным к системе сбора данных и персональному компьютеру.

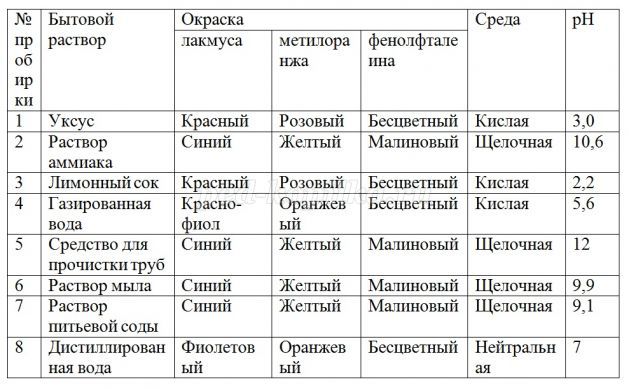
- Самый кислый раствор - это лимонный сок, самый щелочной раствор дает средство для прочистки труб. Следовательно, оба утверждения учителя в игре «Верю - не верю» истинны.
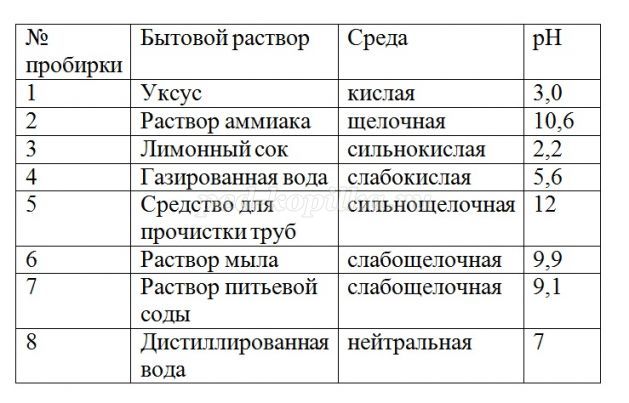
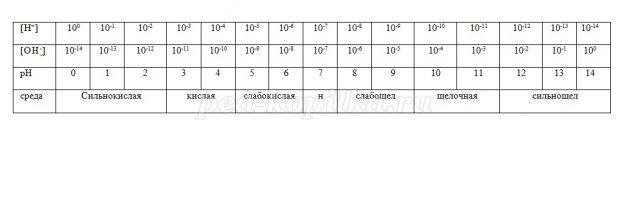
Например:
Водородный показатель.
Точный, диагностичный.
Измеряет, показывает, определяет.
Показатель концентрации ионов водорода. рН
Задание на дом
Проведите домашний эксперимент, выполнив следующие действия: добавьте сок краснокочанной капусты к бытовым растворам (уксуса, раствора аммиака, лимонного сока, газированной воды, средства для прочистки водосточных труб, раствора мыла, раствора питьевой соды) и определите, какой цвет принимает этот индикатор во всём диапазоне рН. Вставьте полученные данные в таблицу, начатую нами на уроке.
Можно ли применять сок краснокочанной капусты как индикатор
для определения силы кислот и щелочей? Поясните.
Перечислите преимущества и недостатки сока краснокочанной капусты как индикатора.
Отвар краснокочанной капусты можно приготовить, сварив её в воде.
Как вариант можно измельчить краснокочанную капусту в блендере,
затем процедить сок.
Скачать Конспект урока химии по теме: «Водородный показатель», 11 класс
Рекомендуем посмотреть:
 Активизация мыслительной деятельности учащихся на уроках литературы средствами ТРКМ
Активизация мыслительной деятельности учащихся на уроках литературы средствами ТРКМ
 Уроки химии для 1 курса колледжа
Уроки химии для 1 курса колледжа
 Конспект урока химии для 11 класса. Факторы, влияющие на скорость химических реакций
Конспект урока химии для 11 класса. Факторы, влияющие на скорость химических реакций
 Конспект урока химии для 11 класса. Химия в жизни человека
Конспект урока химии для 11 класса. Химия в жизни человека
Похожие статьи:
Игра по химии с ответами, 10-11 класс
Применение проблемного обучения на уроках математики
Инновационные подходы к обучению одаренных детей на уроках химии
Участник №43 профессионального конкурса для педагогов на лучшую методическую разработку с 20 июня по 20 сентября 2017 года
|
|
Автор: Елена Александровна Таирова
Опубликовано: 2824 дня назад (15 августа 2017)
Просмотров: 10109
Рубрика: Конспекты уроков
|
+9↑ Голосов: 9 |
| # 21 августа 2017 в 09:42 +7 |
| # 21 августа 2017 в 15:51 +7 | ||
|
| # 21 августа 2017 в 15:51 +7 |
| # 21 августа 2017 в 19:20 +7 |
| # 22 августа 2017 в 15:37 +8 |
| # 26 августа 2017 в 11:22 +5 |
| # 19 октября 2017 в 03:10 +2 | ||
|




